2023年2月28日,《PNAS》在线发表了我院王建军教授课题组题为“The pleiotropic AMPK-CncC signaling pathway regulates the trade-off between detoxification and reproduction”的研究论文。该研究首次揭示了介导昆虫解毒代谢与生殖权衡的分子机制。
生活史理论认为,由于可利用能量资源有限,生物必须在生长发育、生殖和存活间进行权衡和能量合理分配。尤其在环境胁迫条件下,生物通过能量分配使自身适合度最大化,以维持种群的发展。对外源化合物的解毒代谢是昆虫适应环境和对杀虫剂产生抗药性的主要策略之一。由于解毒代谢与生殖都是大量消耗能量的过程,杀虫剂抗性的产生通常以生殖能力下降作为代价,并且在多种昆虫中发现亚致死剂量杀虫剂抑制昆虫生殖,然而长期以来关于介导昆虫解毒代谢与生殖权衡的内在分子机制还知之甚少。
腺苷酸激活蛋白激酶AMPK作为关键的细胞能量感受蛋白,通过抑制合成代谢过程和激活分解代谢过程来调控细胞能量代谢。昆虫Cap ‘n’ collar isoform-C(CncC)是响应外源化合物胁迫的重要转录因子,参与调控解毒代谢相关基因的表达。本研究以赤拟谷盗为模式昆虫,发现溴氰菊酯处理诱导的氧化胁迫上调了AMP:ATP和ADP:ATP的比率,导致AMPK的激活。利用RNA干扰和AMPK激活剂AICAR处理研究发现,AMPK通过影响CncC靶标基因CYP6BQ的表达参与调控赤拟谷盗对溴氰菊酯的耐受性,并且AICAR处理通过影响蜕皮激素和保幼激素的稳态抑制了雌虫生殖。这些研究结果表明AMPK参与了昆虫解毒代谢和生殖的调控。
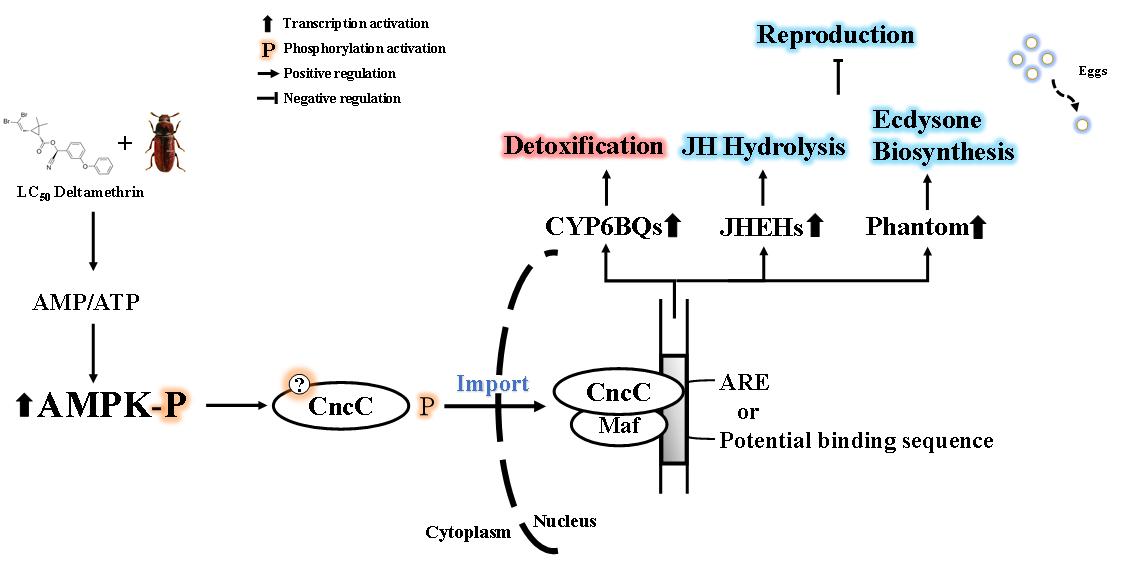
图1 多效性AMPK-CncC信号通路调控赤拟谷盗解毒代谢与生殖权衡模式图
作者在此基础上利用免疫共沉淀、酵母双杂交、GST-Pull Down和BiFC研究发现,AMPK与CncC之间存在互作,并且溴氰菊酯和AICAR处理诱导了CncC核易位,但敲减TcAMPKα减弱了溴氰菊酯诱导的CncC核易位。体外磷酸化试验发现,AMPK能够直接磷酸化CncC,并且利用WB检测发现AICAR、溴氰菊酯处理能够提高体内CncC磷酸化水平,dsTcAMPKα处理能够削弱溴氰菊酯诱导的CncC磷酸化水平。这些研究表明AMPK是CncC的上游调控激酶。
作者进一步利用RNAi分析了CncC对于保幼激素(JH)与蜕皮激素(20E)信号通路相关基因的转录调控,发现敲减TcCncC显著下调20E合成相关基因和JH降解相关基因的表达。双荧光素酶报告基因以及EMSA分析发现,CncC可直接调控20E合成相关基因和JH降解相关基因的表达。
本文研究结果表明,溴氰菊酯诱导的氧化胁迫可以激活AMPK,AMPK通过磷酸化促进CncC入核,导致解毒代谢相关基因的上调表达以及调控生殖的激素水平失衡,表明多效性AMPK/CncC信号通路介导了赤拟谷盗解毒代谢与生殖权衡。审稿专家评论认为该研究为全面认识整个动物界外源化合物及其产生的氧化应激影响生殖的内在机制做出了重要而突出的贡献(“Overall, the studies make an important singular contribution because they establish a mechanistic basis for how xenobiotic and coordinate oxidative stresses can override reproduction across all animal taxa”)。
扬州大学为该论文第一通讯单位,博士研究生姜珩、副教授孟祥坤和博士研究生张楠为共同第一作者,王建军教授、美国堪萨斯州立大学Yoonseong Park教授以及美国肯塔基大学Subba Reddy Palli教授为共同通讯作者。该研究得到国家自然科学基金资助。

 苏公网安备 32100302010246号
苏公网安备 32100302010246号